Ивермектин (Ivermectin) е инхибитор на репликацията на причинителя на COVID-19 (SARS-CoV-2) in vitro
Акценти
- Еднократно третиране с ивермектин е в състояние да намали количеството на вируса в клетъчната култура приблизително 5000 пъти за 48 h
- Ивермектин е одобрен от FDA (Агенцията за контрол на храните и лекарствата на Съединените щати) за борба с паразитни инфекции и затова има потенциал за повторната му поява на пазара
- Ивермектин е широко достъпен благодарение на включването му в списъка на основните лекарства на СЗО (Световната здравна организация)
Теоретични данни
Въпреки че в момента се провеждат няколко клинични проучвания за тестване на възможните терапии с ивермектин, отговорът на пандемията с COVID-19 в световен мащаб до голяма степен е ограничен до ниво мониторинг.
Ивермектин, който е одобрен от FDA като антипаразитно лекарство, показва също така широкоспектърна антивирусна активност in vitro и се проявява като инхибитор на вируса SARS-CoV-2.
След еднократно добавяне на ивермектин към Vero/hSLAM-клетки 2 h след заразяването им със SARS-CoV-2 той е способен да доведе до 5000-кратно намаляване на вирусната РНК за 48 h. Необходими са допълнителни изследвания на ивермектин, за да се установят възможните ползи за хората.
Ивермектин е одобрен от FDA като широкоспектърно антипаразитно средство, което през последните години, заедно с други групи лекарства, показа активност срещу широк спектър от вируси in vitro.
Първоначално е идентифициран като инхибитор на взаимодействието между протеина на интегразата (IN) на човешкия имунодефицитен вирус-1 (HIV-1) и хетеродимера на импортин-алфа/бета-1(IMP-α/β-1), отговорен за ядрения внос на IN. От тогава е потвърдено, че ивермектин инхибира ядрения внос на IN и размножаването на HIV-1.
Има публикации, че ивермектин потиска ядрения внос в гостоприемника на вирусни протеини, включително на големия туморен антиген на полиомавируса (SV40) и неструктурния протеин 5 (NS5) на вируса на денгата (DENV).
Важно е, че е доказано, че ивермектин ограничава инфекцията на РНК-вируси като DENV-1 – 4, западнонилския вирус, венецуелския вирус на енцефалита по конете (VEEV) и грипа, като се смята, че тази широкоспектърна активност се дължи на зависимостта на много различни РНК-вируси от IMP-α/β-1 по време на инфекция. Също така е доказано, че ивермектин е ефективен срещу ДНК на вируса на псевдораби (PRV) както in vitro, така и in vivo, като лечението с ивермектин увеличава преживеямостта на мишки, инфектирани с PVR.
Не е наблюдавана ефективност на ивермектин срещу вируса на зика (ZIKV) при мишки, но учените признават, че поради ограничения брой изследвания е оправдано да се направи повторна оценка на активността на ивермектин против ZIKV.
За финал трябва да отбележим, че през 2014 – 2017 г. ивермектин е бил в центъра на клинично изпитване във фаза III в Тайланд срещу инфекция с DENV, при което е наблюдавано, че еднократната дневна перорална доза е безопасна и води до значително намаляване на серумните нива на неструктурния протеин 1 (NS1), но не са наблюдавани промени във виремията или клиничната полза.
Причинителят на настоящата пандемия COVID-19 (SARS-CoV-2) е едноверижен РНК(+)-вирус, който е тясно свързан с коронавируса, причинител на тежкия остър респираторен синдром (ТОРС) (severe acute respiratory syndrome (SARS)) (SARS-CoV). Проучвания на протеините на SARS-CoV разкриват потенциалната роля на IMP-α/β-1 по време на инфекция от сигналозависимото плазмено затваряне на нуклеокапсидния протеин на SARS-CoV, което може да повлияе на клетъчното деление. Освен това е установено, че допълнителният протеин на SARS-CoV ORF6 антагонизира антивирусната активност на транскрипционния фактор STAT1 чрез секвестриране на IMP-α/β-1 върху мембраната на клетките на ендоплазмения ретикулум (ER) и апарата на Голджи (Golgi). Взети заедно, тези доклади предполагат, че инхибиращата активност на ивермектин може да бъде ефективна срещу SARS-CoV-2.
За да се тества антивирусната активност на ивермектин към SARS-CoV-2, Vero/hSLAM-клетки са инфектирани с изолат на SARS-CoV-2 Australia/VIC01/2020 (MOI = 0.1) и след 2 h са добавени 5 μM ивермектин. Супернатантните и клетъчните култури са събирани в рамките на 3 дни и анализирани с RT-PCR за репликацията на РНК на SARS-CoV-2 (фиг. 1А/В). За 24 h е регистрирано 93% намаление на вирусната РНК, присъстваща в супернатантните (показателно за свободните вириони) проби, третирани с ивермектин, в сравнение с DMSO. По подобен начин е наблюдавано намаление с 99.8% на асоциираната с клетки вирусна РНК (показателно за несвободните и непакетирани вариони) при лечение с ивермектин. След 48 h този ефект се усилва с до 5000-кратно намаление на вирусната РНК при третирани с ивермектин проби в сравнение с контролите, което показва, че ивермектиновото лечение води до ефективно унищожаване практически на целия вирусен материал за 48 h. Според тези проучвания не се наблюдава по-нататъшно намаляване на вирусната РНК след 72 h. Не е наблюдавана токсичност на ивермектин в нито един момент от проучването, нито при пробните сондажи, нито в паралелно тестваните проби само с лекарството.
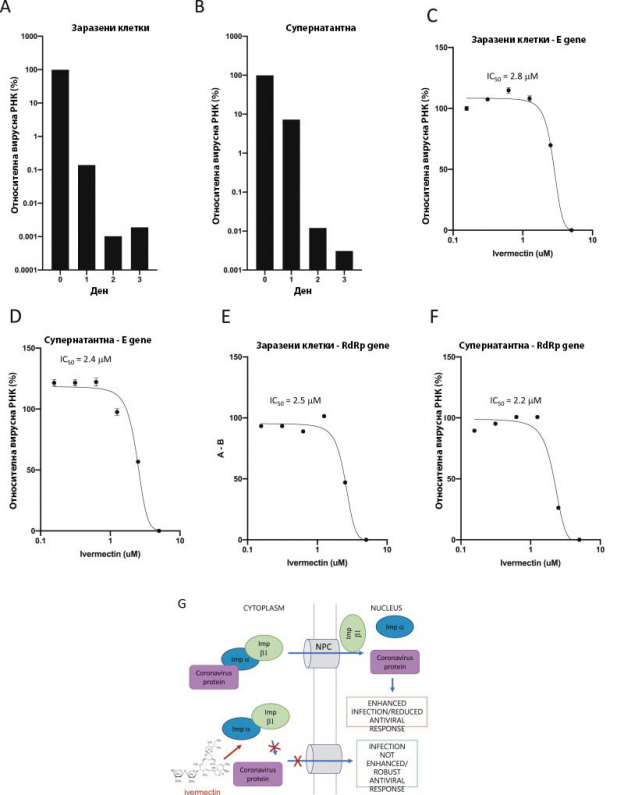
Фиг. 1: Ивермектин е мощен инхибитор на SARS-CoV-2 Australia/VIC01/2020-клиничен изолат
Vero/hSLAM-клетките са инфектирани с клиничен изолат на SARS-CoV-2 Australia/VIC01/2020 (MOI = 0.1) 2 h преди добавянето на DMSO или ивермектин в посочените концентрации.
Пробите са събирани в рамките на 3 дни след инфектирането за количествено определяне на вирусното натоварване посредством RT-PCR на клетъчно асоциирания вирус (фиг. 1А) или супернатант (фиг. 1В). IC50-стойностите са определяни при последващи експерименти 48 h след заразяването, като са използвани указаните концентрации на ивермектин (приложен 2 h след инфектирането съгласно фиг. 1А/В).
Трикратният RT-PCR-анализ е проведен върху клетъчно асоцииран вирус (фиг. 1С/Е) или супернатант (фиг. 1D/F), като са използвани проби срещу гените SARS-CoV-2 E (фиг. 1C/D) или RdRp (фиг. 1E/F). Резултатите представляват средно +/- SD (n = 3). За определяне стойностите на IC50 са конструирани три параметрични криви на отговор на дозата с помощта на GraphPad Prism (фиг. 1G).
Схематично обяснение за антивирусното действието на ивермектин срещу коронавируса: IMP-α/β-1 се свързва с товарния протеин на коронавируса в цитоплазмата (фиг. 1G – горе) и го пренася през ядрения порест комплекс (NPC) в ядрото, където комплексът се разпада и вирусният товар може да намали антивирусната реакция на клетката гостоприемник, което улеснява инфекцията.
Ивермектин се свързва и дестабилизира IMP-α/β-1-хетеродимера, като по този начин предотвратява свързването на IMP-α/β-1 с вирусния протеин (фиг. 1G – долу) и възпрепятства навлизането му в ядрото. Това вероятно резултира в намалено потискане на противовирусния отговор, което води до нормална, по-ефективна антивирусна реакция.
За по-нататъшно определяне на ефективността на ивермектин клетките, заразени със SARS-CoV-2, са третирани със серийни разреждания на ивермектин 2 h след инфекцията и супернатантите и клетъчните посявки, събрани за RT-PCR за 48 h (фиг. 1C/D). Отново е наблюдавано 5000-кратно намаление на вирусната РНК както в супернатантата, така и в клетъчните посявки от проби, третирани с 5 µМ ивермектин за 48 h, което се равнява на 99.98% намаление на вирусната РНК в тези проби.
Отново не е наблюдавана токсичност на ивермектин при някоя от тестваните концентрации. IC50 на лечението с ивермектин е определено да бъде ~ 2 µМ при тези условия.
Подчертавайки факта, че анализът наистина открива конкретно SARS-CoV-2, RT-PCR-експериментите са повтаряни, като са използвани за праймери, специфични за вирусния RdRp-ген (фиг. 1E/F), вместо за Е-гена, при което са наблюдавани почти идентични резултати както за свободния (супернатант), така и за клетъчно асоциирания вирус.
Взети заедно, тези резултати показват, че ивермектин има антивирусно действие срещу клиничен изолат на SARS-CoV-2 in vitro, като една доза може да контролира размножаването на вируса в рамките на 24 – 48 h.
Предполага се, че това вероятно се случва чрез потискане на IMP-α/β-1-медиирания янрен внос на вирусни протеини (фиг. 1G), както е доказано за други РНК-вируси. Потвърждаването на този механизъм в случая на SARS-CoV-2 и/или компонента (компонентите) на клетката домакин е важен фокус в бъдещата работа в лабораториите. В крайна сметка разработването на ефективно противовирусно средство срещу SARS-CoV-2, което да се дава на пациенти в началото на инфекцията, може да помогне за ограничаване на вирусното натоварване, предотвратяване на тежко развитие на болестта и превенция на предаването от човек на човек.
Сравнителното тестване на ивермектин и други потенциални противовирусни средства срещу SARS-CoV-2 с алтернативни механизми на действие би било важно да се случи колкото е възможно по-скоро.
Този кратък доклад открива възможността ивермектин да бъде полезно противовирусно средство за ограничаване на SARS-CoV-2 подобно на тези, за които вече е съобщено. Докато не бъде доказана клиничната им ефективност, всички те трябва да бъдат изследвани възможно най-бързо.
Ивермектин е доказан като безопасен за употреба от човек и е одобрен от FDA (Американската асоциация по храните и лекарствата) за редица паразитни инфекции. Важно е, че последните прегледи и метаанализи показват, че ивермектин във висока доза е безопасен като стандартно лечение с ниски дози. Все още няма достатъчно доказателства, за да се направят окончателни заключения за безопасността на ивермектин по време на бременност.
Най-важната следваща стъпка в по-нататъшната оценка за възможната полза при пациенти със COVID-19 ще бъде изследването на режим на дозиране с множество добавки, който имитира настоящата одобрена употреба на ивермектин при хора. Както беше споменато, ивермектин е бил в центъра на неотдавнашно клинично изпитване във фаза III при пациенти с DENV в Тайланд, което е установило, че една дневна доза е безопасна, но не води до никаква полза. Въпреки това изледователите са отбелязали, че може да се разработи подробен режим на дозиране въз основа на фармакокинетични данни. Въпреки че DENV очевидно е много различен от SARS-CoV-2, това проучване би трябвало да даде информация за бъдещи разработки по-нататък.
Като цяло настоящият доклад, комбиниран с известния профил на безопасност, показва, че ивермектин е достоен за по-нататъшно разглеждане като потенциялно противовирусно средство срещу SARS-CoV-2.
Методика
Клетъчни култури, вирусна инфекция и лечение с лекарства
Vero/hSLAM-клетките се поддържат в минимална есенциална среда на Earle (EMEM), съдържаща 7% фетален говежди серум (FBS), 2 mM L-глутамин, 1 mM натриев пируват, 1500 mg/L натриев бикарбонат, 15 mM HEPES и 0.4 mg/ml генетицин при 37°С, 5% CO2.
Клетките се посяват в 12-гнездни плаки за тъканна култура 24 h преди да бъдат заразени със SARS-CoV-2 Australia/VIC01/2020-клиничен изолат при MOI 0.1 в инфекциозна среда (съдържаща само 2% FBS) за 2 h. Средата, съдържаща инокулум, се отстранява, заменя се с 1 ml свежа среда (2% FBS), съдържаща ивермектин в посочените концентрации или DMSO самостоятелно, и се инкубира, както е посочено, за 0 – 3 дни.
В подходящия момент клетъчният супернатант се събира, завърта се в продължение на 10 min при 6 000 g, за да се отстранят остатъците, и се прехвърля в епруветки за прясно събиране. Клетъчните монослоеве се събират чрез остъргване в 1 ml свежа среда (2% FBS). Контролите на токсичността се задават паралелно във всеки експеримент върху незаразени клетки.
Генериране на SARS-CoV-2-кДНК
РНК се екстрахира от 200 µL аликвоти от супернатанта на пробата или клетъчна суспензия, като се използва QIAamp 96 Virus QIAcube HT kit (Qiagen, Хилден, Германия), и се елуира в 60 µl. Обратна транскрипция се извършва с помощта на комплект BioLine SensiFAST cDNA kit (BioLine, Лондон, Великобритания), обща реакционна смес (20 µl), съсържаща 10 µL екстракт от РНК, 4 µl от 5х буфер TransAmp, 1 µl обратна транскриптаза и 5 µl вода без нуклеаза. Реакциите се инкубират при 25°С за 10 min, 42°С за 15 min и 85°С за 5 min.
Откриване на SARS-CoV-2 с помощта на TaqMan RT-PCR-анализ
TaqMan RT-PCR-анализът се провежда, като се използва 2.5 µl кДНК, 10 µl праймер PrecisionPLUS qPCR Master Mix 1 μM прав (5′- AAA TTC TAT GGT GGT TGG CAC AAC ATG TT-3′), 1 μM обратен (5′- TAG GCA TAG CTC TRT CAC AYT T-3′) праймери и 0.2 μM проба (5′-FAM- TGG GTT GGG ATT ATC-MGBNFQ-3′), насочени към BetaCoV-RdRp-гена (РНК-зависима РНК-полимераза), или прав (5′-ACA GGT ACG TTA ATA GTT AAT AGC GT -3′), 1 µM обратен (5′-ATA TTG CAG CAG TAC GCA CAC A-3′) праймери и 0.2 μM проба (5′-FAM-ACA CTA GCC ATC CTT ACT GCG CTT CG-286 NFQ-3′), насочени към BetaCoV-E-гена.
RT-PCR-тестовете се извършват на Applied Biosystems ABI 7500 Fast RT-PCR (Applied Biosystems, Фостър Сити, Калифорния, САЩ) при използване на циклични условия от 95°C за 2 min, 95°C за 5 sec, 60°C за 24 sec. Като положителна контрола се използва SARS-CoV-2-кДНК (Ct ~ 28).
Изчислените стойности на Ct се преобразуват в намаление на кратността на третираните проби в сравнение с контролата по метода ΔCt (кривата се променя във вирусна RNA = 2^ΔCt) и се изразяват като % от самостоятелна проба с DMSO.
Стойностите на IC50 се монтират с помощта на 3 параметрични криви на отговор на дозата в GraphPad Prism.
- Етикети:
- Рубрики: