Спайквакс (Ваксина срещу COVID-19 Модерна) инжекционна дисперсия, иРНК ваксина срещу COVID-19 (нуклеозидно модифицирана)
Spikevax (COVID-19 Vaccine Moderna) dispersion for injection, COVID-19 mRNA Vaccine (nucleoside modified)
- Приложение при деца: Безопасността и ефикасността на Спайквакс (Spikevax) при деца и юноши на възраст под 12 години все още не са установени
- Приложение при пациенти на(д) 65 години: Не се изисква корекция на дозата при лица в старческа възраст ≥ 65 години
- Приложение при бременност: Приложението на Спайквакс (Spikevax) по време на бременност трябва да се обмисля само когато потенциалните ползи надхвърлят всякакви потенциални рискове за майката и фетуса
- Приложение при кърмене: Не е известно дали Спайквакс (Spikevax) се екскретира в кърмата
- Приложение при опити за забременяване: Проучвания при животни не показват преки или непреки вредни ефекти, свързани с репродуктивна токсичност
- Приложение при шофиране и работа с машини: Спайквакс (Spikevax) не повлиява или повлиява пренебрежимо способността за шофиране и работа с машини
Фармакодинамика
Спайквакс (Spikevax) съдържа иРНК, включена в липидни наночастици. иРНК кодира пълноверижен шипов протеин на SARS-CoV-2, модифициран с 2 пролинови замествания в областта на хептадното повторение 1 (S-2P) за стабилизиране на шиповия протеин в префузионна конформация. След интрамускулна инжекция клетките на мястото на инжектиране и дрениращите лимфни възли поемат липидните наночастици, като ефективно доставят иРНК секвенцията в клетките за транслация във вирусен протеин. Доставената иРНК не навлиза в клетъчното ядро и не взаимодейства с генома, не се репликира и се експресира временно основно в дендритни клетки и макрофаги в субкапсуларните синуси. Експресираният, свързан с мембраната шипов протеин на SARS-CoV-2 се разпознава след това от имунните клетки като чужд антиген. Това предизвиква както Т-клетъчен, така и В-клетъчен отговор с образуване на неутрализиращи антитела, което може да допринесе за защитата срещу КОВИД-19 (COVID-19).
Показания
Спайквакс (Spikevax) е предназначена за активна имунизация за превенция на КОВИД-19 (COVID-19), причинен от SARS-CoV-2, при лица на 12 и повече години в съответствие с официалните препоръки.
Противопоказания
Свръхчувствителност към активното вещество или към някое от помощните вещества:
- Липид SM -102
- Холестерол
- 1,2-дистеароил-sn-глицеро-3-фосфохолин (DSPC)
- 1,2-димиристоил-rac-глицеро-3-метоксиполиетиленгликол-2000 (PEG2000 DMG)
- Трометамол
- Трометамол хидрохлорид
- Оцетна киселина
- Натриев ацетат трихидрат
- Захароза
- Вода за инжекции
Специални предупреждения и предпазни мерки
Проследимост
За да се подобри проследимостта на биологичните лекарствени продукти, името и партидният номер на приложения продукт трябва ясно да се записват.
Свръхчувствителност и анафилаксия
Има съобщения за анафилаксия. Винаги трябва да има на разположение подходящо медицинско лечение и наблюдение в случай на анафилактична реакция след приложение на ваксината. Препоръчва се внимателно наблюдение в продължение на най-малко 15 минути след ваксинацията. Втората доза на ваксината не трябва да се поставя на онези, които са получили анафилаксия при първата доза на Спайквакс (Spikevax).
Миокардит и перикардит
След ваксинация със Спайквакс (Spikevax) са наблюдавани много редки случаи на миокардит и перикардит. Тези случаи са настъпили предимно в рамките на 14 дни след ваксинация, по-често след втората ваксина и по-често при по-млади мъже. От наличните данни може да се предположи, че протичането на миокардит и перикардит след ваксинацията не се различава от това при миокардит или перикардит като цяло.
Медицинските специалисти трябва да бъдат бдителни за признаците и симптомите на миокардит и перикардит. Ваксинираните лица трябва да бъдат инструктирани да потърсят незабавно медицинска помощ, ако развият симптоми, показателни за миокардит или перикардит, като (остра и продължителна) болка в гърдите, задух или палпитации след ваксинацията.
Медицинските специалисти трябва да направят справка с ръководствата и/или специалистите за диагностициране и лечение на това заболяване.
Рискът от миокардит след трета доза (0.5 ml, 100 микрограма) или след бустер доза (0.25 ml, 50 микрограма) Спайквакс (Spikevax) все още не е охарактеризиран.
Реакции, свързани с тревожност
Реакции, свързани с тревожност, включително вазовагални реакции (синкоп), хипервентилация или такива, свързани със стрес, могат да се появят във връзка с ваксинацията като психогенен отговор към инжектирането с игла. Важно е да се вземат предпазни мерки, за да се избегне нараняване при прилошаване.
Съпътстващо заболяване
Ваксинацията трябва да се отложи при лица, страдащи от остро тежко фебрилно заболяване или остра инфекция. Наличието на лека инфекция и/или леко повишена температура не трябва да забавя ваксинацията.
Тромбоцитопения и нарушения на кръвосъсирването
Както при други интрамускулни инжекции, ваксината трябва да се прилага внимателно при лица на антикоагулантна терапия или такива с тромбоцитопения или някакво нарушение на кръвосъсирването (например хемофилия), тъй като при тези лица може да се появи кървене или образуване на синини след интрамускулното приложение.
Имунокомпрометирани лица
Ефикасността и безопасността на ваксината не са оценени при имунокомпрометирани лица, включително такива, получаващи имуносупресивна терапия. Ефикасността на Спайквакс (Spikevax) може да бъде по-ниска при имунокомпрометирани лица.
Препоръката да се обмисли приложение на трета доза (0.5 ml) при тежко имунокомпрометирани лица се основава на ограничени серологични данни при пациенти, които са имунокомпрометирани след трансплантация на солиден орган.
Продължителност на защитата
Продължителността на осигурената от ваксината защита е неизвестна, тъй като тя все още се установява от текущи клинични изпитвания.
Ограничения на ефективността на ваксината
Лицата може да не бъдат напълно защитени до 14-ия ден след поставяне на втората доза. Както при всички ваксини, ваксинацията със Спайквакс (Spikevax) може да не осигури защита на всички реципиенти на ваксината.
Помощни вещества с известно действие
Натрий
Тази ваксина съдържа по-малко от 1 mmol натрий (23 mg) на 0.5 ml доза, т.е. може да се каже, че на практика не съдържа натрий.
Приложение
Дозировка
Първична серия на ваксинация
Лица на 12 и повече години
Спайквакс (Spikevax) се прилага като курс от 2 (две) дози по 100 микрограма (0.5 ml всяка). Препоръчва се втората доза да се приложи 28 дни след първата доза.
Бустер доза
Лица на 18 и повече години
Една бустер доза (0.25 ml, съдържаща 50 микрограма иРНК – половината от първичната доза) Спайквакс (Spikevax) може да се приложи интрамускулно най-малко 6 месеца след втората доза на лица на 18 и повече години. Решението кога и на кого да се приложи трета доза Спайквакс (Spikevax) трябва да се вземе въз основа на наличните данни за ефективността на ваксината, като се имат предвид ограничените данни за безопасност.
Взаимозаменяемостта между Спайквакс (Spikevax) и други ваксини срещу КОВИД-19 (COVID-19) за завършване на първичния курс на ваксинация или за поставяне на бустер доза (0.25 ml, 50 микрограма) не са установени. Лицата, които са получили една доза Спайквакс (Spikevax) (0.5 ml, 100 микрограма), трябва да получат втора доза Спайквакс (Spikevax) (0.5 ml, 100 микрограма), за да се завърши първичният курс на ваксинация.
Тежко имунокомпрометирани лица на 12 и повече години
На лица, които са тежко имунокомпрометирани, трета доза (0.5 ml, 100 микрограма) може се приложи най-малко 28 дни след втората доза.
Педиатрична популация
Безопасността и ефикасността на Спайквакс (Spikevax) при деца и юноши на възраст под 12 години все още не са установени. Липсват данни.
Популация в старческа възраст
Не се изисква корекция на дозата при лица в старческа възраст ≥ 65 години.
Начин на приложение
Ваксината трябва да се прилага интрамускулно. За предпочитане е в делтоидния мускул в горната част на ръката.
Не прилагайте тази ваксина интраваскуларно, подкожно или интрадермално.
Ваксината не трябва да се смесва с други ваксини или лекарствени продукти в същата спринцовка.
Предозиране
Не са съобщени случаи на предозиране.
В случай на предозиране се препоръчва проследяване на жизнените функции и възможно симптоматично лечение.
Срок на годност
Неотворен флакон
7 месеца при температура от -25ºС до -15ºC.
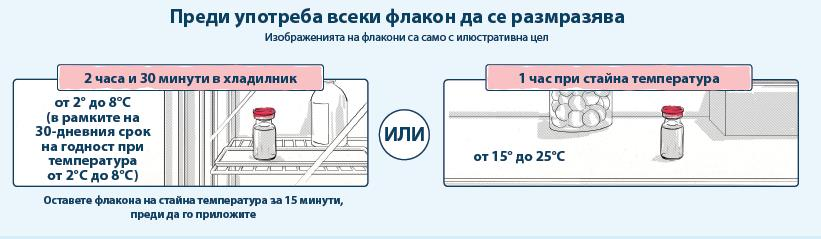
Неотворената ваксина може да се съхранява в хладилник при температура от 2°C до 8°C, защитена от светлина, максимум за 30 дни. В рамките на този период за транспортиране могат да се използват до 12 часа.
Веднъж размразена, ваксината не трябва да се замразява повторно.
Неотворената ваксина може да се съхранява при температура от 8°C до 25°C до 24 часа след изваждане от хладилник.
Пунктиран флакон
Доказана е химична и физична стабилност при употреба в продължение на 19 часа след първоначалното пунктиране при 2°C до 25°C (в рамките на периода, позволен за употреба, който е 30 дни при температура от 2°C to 8ºC и 24 часа при температура от 8°C to 25ºC). От микробиологична гледна точка продуктът трябва да се използва незабавно. Ако ваксината не се използва веднага, периодът на използване и условията на съхранение преди употреба са отговорност на потребителя.
Специални условия на съхранение
Да се съхранява във фризер при температура между -25°C и -15°C.
Да се съхранява в оригиналната опаковка, за да се предпази от светлина.
Да не се съхранява в сух лед или под -50°C.
Транспортиране на размразени флакони в течно състояние при температура от 2°C до 8°C
Ако транспортирането при температура от -50°C to -15°C не е възможно, налични са данни, според които е възможно транспортирането на един или повече размразени флакона в течно състояние за период до 12 часа при температура от 2°C до 8°C (в рамките на 30-дневния срок на годност при температура 2°C до 8°C). Веднъж размразени и транспортирани в течно състояние при температура от 2°C до 8°C, флаконите не трябва да се замразяват повторно, а да се съхраняват при температура от 2°C до 8°C до тяхното използване.
Вид и съдържание на опаковката
5 ml дисперсия във флакон (стъкло тип 1 или еквивалент) със запушалка (хлоробутилов каучук) и обкатка (алуминий) с отчупващо се пластмасово капаче.
Всеки флакон съдържа 5 ml.
Съдържание на опаковката: 10 многодозови флакона.
Специални предпазни мерки при изхвърляне и работа
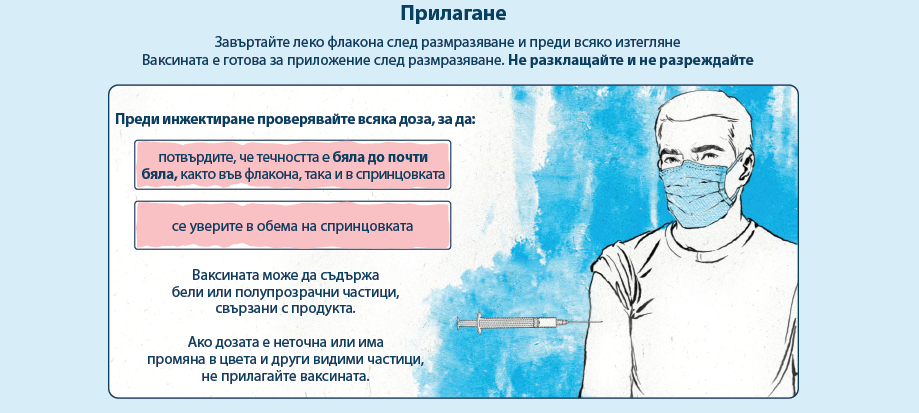
Ваксината трябва да се приготвя и поставя от обучени медицински специалисти при спазване на асептични техники, за да се гарантира стерилност на дисперсията.
Ваксината е готова за употреба след размразяване.
Да не се разклаща или разрежда. Завъртете леко флакона след размразяване и преди всяко изтегляне.
Флаконите със Спайквакс (Spikevax) са многодозови.
От всеки флакон могат да се изтеглят десет (10) дози (по 0.5 ml всяка) или максимум двадесет (20) дози (по 0.25 ml всяка).
Препоръчително е да пробождате запушалката на различно място всеки път. Не пунктирайте флакона повече от 20 пъти.
Във всеки флакон се съдържа излишък, за да може да се гарантира доставянето на 10 дози по 0.5 ml всяка или максимум 20 дози по 0.25 ml.
С размразени флакони и пълни спринцовки може да се работи при условия на стайно осветление.


Бременност
Има ограничен опит с използването на Спайквакс (Spikevax) при бременни жени. Проучвания при животни не показват преки или непреки вредни ефекти, свързани с бременността, ембрионалното/феталното развитие, раждането или постнаталното развитие. Приложението на Спайквакс (Spikevax) по време на бременност трябва да се обмисля само когато потенциалните ползи надхвърлят всякакви потенциални рискове за майката и фетуса.
Кърмене
Не е известно дали Спайквакс (Spikevax) се екскретира в кърмата.
Фертилитет
Проучвания при животни не показват преки или непреки вредни ефекти, свързани с репродуктивна токсичност.
Шофиране и работа с машини
Спайквакс (Spikevax) не повлиява или повлиява пренебрежимо способността за шофиране и работа с машини. Някои от нежеланите реакции, посочени по-долу, могат все пак временно да повлияят на способността за шофиране или работа с машини.
Взаимодействия
Не са провеждани проучвания за взаимодействията.
Не е проучвано съпътстващото приложение на Спайквакс (Spikevax) с други ваксини.
Нежелани реакции
Съобщените нежелани реакции са изброени според следната конвенция за честота:
- Много чести (≥ 1/10)
- Чести (≥ 1/100 до < 1/10)
- Нечести (≥ 1/1000 до < 1/100)
- Редки (≥ 1/10 000 до < 1/1000)
- Много редки (< 1/10 000)
- С неизвестна честота (от наличните данни не може да бъде направена оценка)
В рамките на всяко групиране по честота нежеланите реакции са представени в низходящ ред по отношение на сериозността.
| Системо-органен клас по MedDRA | Честота | Нежелана(и) реакция(и) |
|---|---|---|
| Нарушения на кръвта и лимфната система | Много чести | Лимфаденопатия * |
| Нарушения на имунната система | С неизвестна честота |
Анафилаксия Свръхчувствителност |
| Нарушения на нервната система | Много чести | Главоболие |
| Нечести | Замаяност | |
| Редки |
Остра периферна лицева парализа ** Хипестезия |
|
| Сърдечни нарушения | Неизвестна честота |
Миокардит Перикардит |
| Стомашно-чревни нарушения | Много чести | Гадене/повръщане |
| Нарушения на кожата и подкожната тъкан | Чести | Обрив |
| Нарушения на мускулно-скелетната система и съединителната тъкан | Много чести |
Миалгия Артралгия |
| Общи нарушения и ефекти на мястото на приложение | Много чести |
Болка на мястото на инжектиране Умора Втрисане Пирексия Подуване на мястото на инжектиране |
| Чести |
Еритем на мястото на инжектиране Уртикария на мястото на инжектиране Обрив на мястото на инжектиране Реакция на мястото на инжектиране от забавен тип |
|
| Нечести | Пруритус на мястото на инжектиране | |
| Редки | Подуване на лицето *** | |
| * Лимфаденопатия е била установена като аксиларна лимфаденопатия от същата страна на мястото на инжектиране. В някои случаи са засегнати и други лимфни възли (напр. шийни, надключични). | ||
| ** В рамките на периода на проследяване на безопасността се съобщава за остра периферна лицева парализа при трима участници в групата на Спайквакс (Spikevax) и при един пациент в групата на плацебо. Появата при пациентите в групата на ваксината настъпва след 22, 28 и 32 дни след ваксинацията с доза 2. | ||
| *** Има две сериозни нежелани събития на подуване на лицето при реципиенти на ваксината с анамнеза за инжектиране на дермални филъри. Появата на подуването е съобщено съответно 1 и 2 дни след ваксинацията. | ||
- Производител/Вносител:
- Показания:
Покана
Ако сте медицински, здравен или сроден специалист и бихте желали да допринесете за подобряване качеството на тази публикация – да предложите свой собствен авторски текст, фотография или видео, или просто да ни посочите грешка от едно или друго естество, която може да сме допуснали при подготовката на материала, заповядайте!